Los puntos de fusión y de ebullición son dos constantes físicas muy usadas y pedidas en los cursos de Química y Física.
Punto de Fusión: Es la temperatura en la cual se verifica el cambio de estado físico de solido a liquido. Por ejemplo el hielo que se derrite y se transforma en agua líquida a 0°C a una atmósfera o 760 mm de Hg (mercurio) de presión . Cada sustancia tiene su punto o temperatura de fusión propia. Otro ejemplo lo constituyen los metales que también tienen una temperatura específica en la cual comienzan a pasar al estado líquido.
Punto de ebullición: Es la temperatura en la cual se verifica el pasaje del estado líquido al estado de vapor o gas. Volviendo al ejemplo del agua, lo podemos observar cuando pasa de agua líquida a vapor de agua. En este caso el punto es de 100 °C siempre y cuando la presión sea del valor de una atmósfera.
Como vemos el valor de los puntos de fusión y ebullición están afectados por el valor de la presión atmosférica. Es decir depende de esta. Por norma siempre se verán los valores en las tablas de estas constantes que están referidas o medidas a 1 atmósfera.
La importancia de saber los valores de los puntos de ebullición y de fusión tiene que ver con la identidad de una sustancia. Por ejemplo, el punto de fusión del aluminio es de 660,3 °C. No hay otra sustancia que tenga exactamente este mismo punto de fusión lo cual le da una gran importancia a la identidad del aluminio como tal. Lo mismo pasa con los puntos de ebullición. Estas constantes son propiedades intensivas como hemos explicado el concepto de las propiedades intensivas como aquellas que no varían con la cantidad de materia.
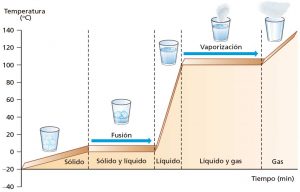
Otra característica muy importante que deben saber es que mientras se produce un pasaje o cambio de estado las temperaturas de fusión y de ebullición se mantienen constantes. Hasta que el cambio de estado llegue a su fin. Recién en el nuevo estado físico las temperaturas podrán variar hasta otro nuevo cambio de estado. En el siguiente gráfico podemos observar con detalle los cambios físicos en el agua. Como podrán observar, a los 0°C y a los 100° C se producen los cambios de estado y las temperaturas permanecen constantes mientras duran dichos cambios. Este tipo de gráficas es muy similar para todas las sustancias.
No te pierdas el siguiente video y te quitarás todas las dudas.

como se resuelve la siguiente ecuación? alguien me pude ayudar por favor se los agradecere
sen x / cos x= cos x / 1+sen x
tan x – sen x / sen3x= secx / 1+cosx
por acá es muy complicado contestarte ecuaciones. Aparte estás en el post equivocado. Por si te interesa te dejo mi mail [email protected] prestamos servicio de rsolución de problemas y trabajos prácticos antes lo cotizamos.
6-¿Cuales características corresponden a compuestos covalentes polares? Justifique
A-Bajos puntso de fusión y ebullición
B-Las moléculas de H y Cl pertenecen a este grupo
C- Conducen la corriente eléctrica en disolución acuosa
C
la A. La c corresponde a los ionicos.
ya pa q
no seee xddd
Qué significa que 2 sustancias distintas, en mismas condiciones de temperatura y presión, tengan el mismo punto de fusión?
Sabes que no conozco a dos sustancias que tengan el mismo punto de fusión y menos en las mismas condiciones de temperatura y presión. Es más, son propiedades intensivas lo cual ayuda a identificar a las diferentes sustancias gracias a estas propiedades.
tu que sabes
Lo que se y lo transmito.
No conozco a dos sustancias que lleguen a eso. Podes darme algún ejemplo?.
6-¿Cuales características corresponden a compuestos covalentes polares? Justifique
A-Bajos puntso de fusión y ebullición
B-Las moléculas de H y Cl pertenecen a este grupo
C- Conducen la corriente eléctrica en disolución acuosa
Podría ser que una de las sustancias o las dos sean mezclas, no sean sustancias puras, o que alguna o las dos de ellas tengan impurezas que influyen en el punto de ebullición y de fusión.
Característica que indica los puntos de fusion y ebullicion de las sustancias, ¿Cuál es?
A que te refería con característica?.
Hola cuál es la respuesta de “punto de fusión y de ebullición de 6 sustancias diferentes»
Busca 6 sustancias y ponele sus puntos de fusión y ebullición.
El cambio de estado.
Los puntos de fusion y ebullicion de un material son propiedades extensivas o intensivas?
Creo que lo dije en el video Agus. Son propiedades intensivas.
Cuál tiene mayor punto de fusión entre el SO2 y el MgO y porqué?
Averigualo en google.
Cuando calentamos naftaleno para derretirlo, la temperatura de fusion es mayor que si agregamos otra sustancia. si hacemos esto y tenemos al naftaleno con azufre, por ejemplo, la temperatura de fusion baja?
Si baja por tratarse de propiedades coligativas.
Cuáles son los puntos en química, como el de ebullicion, fusión pero cuáles otros existen
Los puntos de ebullición y de fusión varían según la sustancia. Esos datos se buscan en tablas.
Hola, En primer lugar maravillosa la explicación. Mi consulta es la siguiente podría usted hacer el mismo ejemplo, pero con aceite y alcohol.
Muchas Gracias por ser tan didáctico.
No cambiará nada solo los números. Gracias.
me puedes responder a esta pregunta?
Averigua los valores de las T de ebullición y fusión de compuestos químicamente similares al agua. Son cercanos a la T ebullición y fusión de la misma? ¿Por qué?
Es un trabajo de investigación. Lo debes hacer tu Anabel.
El punto de congelacion del agua varia connla presion al igual que el punto de ebullicion??
Así es Luis. Abrazo. Te dejo mi canal de youtube. Entra y verá mucho material.
https://www.youtube.com/channel/UCWzKIkF6_U4poswb9qgfVgQ
A que se debe el valor aparentemente anomalo del agua ( 0° de fusion y 100° de ebullicion)? Si en funcion de su masa molecular los valores de estos serian distintos, como pasa con los demas hidruros del grupo 6A.
Tengo una tarea y en una pregunta de esa tarea dice lo siguiente:
¿De que características químicas moleculares de una sustancia depende el punto de fusión? Proporcione al menos 2 ejemplos
Y por lo que eh estado investigando, en todos los post, las paginas y demás solo hablan de que es un solido la sustancia y que el punto de fusión es cuando pasa de solido a liquido a una temperatura constante, en ningún momento mencionan las características que debe de tener la sustancia.
¿Podrías por favor ayudarme?
Hola Brandom. Es importante el tipo d eunión entre sus átomos. Por ejemplo los compuestos iónicos presentan mayores puntos de ebullición y fusión que los compuestos covalentes ya que los i´nicos presentan uniones más fuertes entre sus iones. Entiendes?.
Hola necesito 5 caracteristicas de temperatura de ebullicion, me podrias ayudar?
Nosé a que te referís. No hay características en particular de T de ebullición.
Entonces los metales tienen temperaturas de ebullicion y fusion
Bajas
Altas
O
Medias
Me podrias ayudar
Altas
el oro y el benceno almacenados a 273° en que estado de la materia quedarian
tenes que fijarte los puntos de fusión y ebullición para eso. Pasamelos y vemos.
cuales son las propiedades de punto de ebullicion
No hay propiedades en si del punto de ebullición. A que te refieres?.
Me puedes ayudar.
Trato de entender entonces que, los p. de fusión y ebullición van a disminuir de arriba hacia abajo debido a que los átomos serán más grandes y tenemos mayor facilidad de romperlo.
Estoy en lo cierto o corregime, gracias
átomos más grandes?. Explicame a que sustancias te referis.
todos los materiales tiene el mismo punto de ebullicion?
No Cristian. Cada sustancia tiene su propio punto de ebullición.
Buenas tengo una duda
Existen tipos de punto de ebullición
Y cuales son
Gracias
Hola, no. El punto de ebullición es eso.
Hola, cual seria la formula para saber el punto de fusión y ebullición de un elemento?
No hay fórmula para eso. Hay constantes que se determinaron empiricamente, o se, por experimentos.
Hola, tengo una duda existencial y temo que sea tonta, pero acá va:
El punto de ebullición del agua es de 100 ºC (a 1 ATM), en eso estoy de acuerdo, y lo explico así: la temperatura del agua debe elevarse hasta 100 grados centígrados para llegar a ebullición. Pero no entiendo cuando una sustancia tiene puntos de ebullición negativos, ¿qué significa? No puede ser que «hierva a temperatura de congelación», no lo comprendo y sé que quizá estoy errando en los conceptos. Por ejemplo: H2S tiene un punto de ebullición de -62 º-C.
Espero que pueda responderme.
Saludos y gracias!
Hola Belén. Hay sustancias que pasan de líquido a gas o vapor a temperaturas bajas como el ejemplo que diste. Es natural aunque te paresca extraño. Pasa en los gases. A temperatura ambiente son gases entonces te preguntás a que temperatura paso de líquido a vapor?. Es normal.
¿se podría utilizar otro liquido de calentamiento diferente al aceite mineral?
¿Para que?.
Hola!
Mi preguntas es: ¿Como es la variación de el P. Ebullición y P. Fusión entre diferentes sustancias?
¿El P. Ebullición y P. Fusión de que depende ?
¿Como varia el P. Ebullición y P. Fusión entre sustancias orgánicas y sustancias inorgánicas?
Hola Santiago. Depende de varios factores. Por ejemplo en el agua los puntos son altos porque las moléculas están unidas por enlaces puentes de hidrógeno que son fuertes. Entonces para romperlos hay que elevar la temperatura considerablemente. Esa regla se cumple en todas las sustancias polares como el agua. Las no polares tienen puntos más bajos.
Hola, necesito el punto de ebullición de la clorhexidina ya que no aparece en ningún lado, si me pueden ayudar sería lo ideal
Hola, necesito saber por qué disminuye la temperatura de fusión y la temperatura de ebullición desde el Hierro hacia el Níquel?
Alguien me puede ayudar con esto?
Hola químico, tengo una pregunta, pues he estado leyendo varios artículos pero ninguno responde mi duda, ¿como determinar el punto de fusion mas alto si tiene el mismo peso molecular? Le agradecería mucho que me explicara.
No entiendo la pregunta Beatríz.
Hola,¿cuáles son las reacciones quimicas del aire?
Hola. No tienen reacciones específicas.
necesito informacion de puntos de fusion y ebullicion
No leístes el artículo?.
por que el punto de ebullicion y fusiòn del agua sean comparativamente elevados?
Elevados con respecto a que?.
Buenas tardes
¿De qué depende el punto de ebullición en los compuestos orgánicos?
Como se determina el promedio de un punto de ebullición de un líquido que se ha medido cinco veces?
¿Por qué las sustancias tienen distinto punto de ebullición o fusión? Me refiero por ejemplo, a por qué una sustancia ebulle a 100° y otra a 96°?
Hola Ignacio. Depende de muchos factores. El tipo de molécula si es iónica o covalente o si presentan puentes de hidrógeno etc.
cual es el punto de ebullición del que-rosen, gas, diésel, lubricante
Google.
una sustancia que tiene una densidad de 0.2 g/ml y una masa de 40 gramos, tiene un volumen de: *
8 ml
80 ml
800 ml
ninguna es correcta
Ninguna. Tenes que despejar el Volumen de la formula de densidad. V = masa/densidad.
Tanto el punto de fusión como el punto de ebullición son
A )propiedades especificas de la materia
B) propiedades organolepticas de la materia
C) propiedades extensivas de la materia
D)propiedades intensivas de la materia
E)ninguna de las opciones es correcta
D)
Si cuento con una material que tiene un punto de fusión de 85°C y un punto de ebullición de 153°C. Cuando se encuentre a los 100 °C, su estado será.
Líquido obviamente.
Explique ¿por qué la temperatura de fusión no depende de la presión ambiental y la de ebullición si?
Estoy un poco confundida con esa pregunta ya que estaría negando lo expresado en este artículo me podría ayudar?
Si depende.
caracteristicas de la crema dental y los fertilizantes en terminos ionicos
hola buenas tardes, tengo una consulta respecto a los puntos de fusion y ebullision del agua
¿porque tienden a ser valores mas altos de lo esperado?
me podria ayudar, disculpa la molestia, graciass!!!
Hola. Porque a lo esperado?. Que esperabas?.
Hola! Tengo una consulta, ¿Por qué algunas temperaturas de fusión tienen valores negativos? Pregunté a otra persona pero no logré entenderle. Espero su respuesta, gracias!
Hola Valentina. Se da en los gases porque sus moléculas están muy separadas por su estado físico. Entonces para que lo pases a sólido imaginate cuanto tenes que bajar la temperatura. Entendés?.
¿qué importancia tiene el punto de fusión para los seres vivos?
No veo ninguna. Es más si estaríamos en el punto de fusión del agua estaríamos muertos. Porque nos congelaríamos.
Con que objetivo se debe conocer el punto de fusión y ebullición de las diferentes sustancias?
Es fundamental para conocer sus propiedades y como actúan a distintas temperaturas.
cual es la relacion entre el punto de fusion y los puentes de hidrogeno
Buena pregunta Edgar. Exactamente no sabría decirte. Debería averiguar.
Me pueden ayudar con esta pregunta por favor
Que tiene los siguiente valores
Densidades de:
Punto de ebullición de:
Punto de fusión de:
Y la pregunta? jajaja
¿Cómo son las temperaturas de fusión y de ebullición para cada
elemento?
Cada elemento tiene la suya.
cual elemento tiene mayor punto de fusion y cual tiene menor punto de ebullicion explique a que se debe
Deberás averiguarlo en alguna tabla.
Me podría regalar su apellido para citarlo en un trabajo
Hola. Profesor y Bioquímico Patricio Arroyo.
Analice los resultados de la determinación del punto de fusión explique el comportamiento cuando a la muestra se le adiciona almidón
punto de fusión de que?.