La fórmula del ozono es O3, es decir, la molécula esta formada por tres átomos de oxígeno unidos entre si por uniones covalentes. Lo cual nos permite decir que el ozono es una variedad alotrópica del oxígeno. Alotropía es las distintas formas en las que un mismo elemento se puede presentar, en este caso O2 (oxígeno) y O3 (ozono).
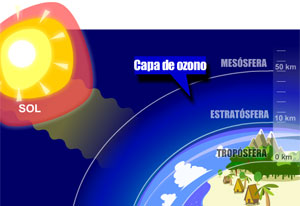
Historia: En 1839 Schönbein comprobo que luego de las tormentas eléctricas se percibia un olor característico como a fósforo. Posteriormente Von Siemens fue el primero en fabricarlo a partir de descargas eléctricas en tubos especiales llamados ozonizadores. En 1864 Soret estableció su fórmula (O3). Se halla en la atmósfera naturalmente pero en muy pequeña proporción. Esta formando una capa afuera de la atmósfera llamada capa de ozono que es la protectora de los rayos UV. No dejando pasar o disminuyendo notoriamente el pasaje de estos rayos a nuestro planeta. Sabemos que esa capa de ha ido deteriorando desde hace mucho por la actividad industrial y genera mucha preocupación el aumento en la concentración de los rayos UV que son los responsables del cáncer de piel.
Métodos de obtención:
Como se menciono antes, se lo prepara por descargas eléctricas sobre el aire u oxígeno en un ozonizadosr de Siemens.
Otro método es por una reacción química. El ácido sulfúrico actúa sobre el permanganato de potasio.
2 KMnO4 + 4 H2SO4 —-> 2 KHSO4 + 2 MnSO4 + 3 H2O + O3 + O2
Propiedades del Ozono:
Es un gas de olor fosforado, más denso y activo quimicamente que el oxígeno. Tiene propiedades bactericidas. Se descompone según la reacción:
O3 —> O2 + O
Oxida a casi todos los metales.
Identificación del ozono:
Para identificarlo se usan unos papeles especiales llamados ozonoscópicos. son papeles de filtro impregnados con oduro de potasio y engrudo de almidón. Si hay ozono se produce la siguiente reacción:
O3 + 2 KI + H2O —> O2 + 2 KOH + I2
El yodo liberado azulea al almidón.
Usos del Ozono:
Se usa para purificar el agua y otros ambientes que necesitan esterilidad por su poder bactericida.
Por la misma razón se usa como conservante de algunos alimentos.
En el blanqueo de telas u otros materiales por su elevado poder oxidante, que se ve por su gran acción deoclorante.
En muchas enfermedades se esta utilizando en una terapia llamada ozonoterapia para tratar muchas enfermedades de distintos orígenes y cuadros como enfermedades inflamatorias como artritis óseas, hepáticas y neurológicas entre otras. Quizá no de la cura, pero alivia los dolores en gran medida y eso mejora la calidad de vida de los pacientes. El ozono una vez introducido al organismo desencadena una serie de reacciones metabolicas positivas que ayudan a combatir a todos estos trastornos.
gracias Patricio, soy un estudiante de preparatoria y tu información es de gran utilidad! gracias
Reaccion quimica de los nitritos con el ozono?
Muy Buena info , me sirvió mucho para una prueba. Gracias!
Nos alegramos Elias
Buenos días,¿ es útil el ozono utilizándolo como fumigación para ahuyentar roedores?
No lo sé pero podría funcionar. Inténtalo y coméntalo.
El ozono oxida las gomas?
Es probable. Es un oxidante fuerte.
cuales son las contraindiccaciones de inyectarse ozono en la sangre
Hola. La verdad desconozco los efectos colaterales. Pero creo que no debe ser tan perjudicial si lo administra un profesional que sepa y sea bien serio.
Hay algún método de medir los ppm de ozono en agua ozonificada ??
No lo sé.
Alguien me podría responder la siguiente pregunta: Si el Ozono es mas denso que el Oxigeno, ¿Por qué el ozono tiende a estar en la estratosfera y el oxigeno al nivel del mar, si el ozono es mas denso que el oxigeno, ya que en teoría si dos gases o fluidos que están en una atmósfera de cualquier tipo, el fluido mas denso tiende estar en la parte inferior de la atmósfera y el mas ligero en la parte superior?
se que es una extraña pregunta, pero se me hizo muy interesante cuando me la hicieron.
Saludos
Patricio revisa una empresa taiwanesa llamada Cashido Corp, te podria ayudar mucho
Hola Luis. ¿Porque lo dices?.
Hola, me interesa saber si el ozono puede ayudar a eliminar o reducir los agroquímicos de verduras y frutas. Gracias.
Hola Oscar. No veo como. Igual dejamos tu inquietud para saber si alguien puede aportar algo.
Porque no son gases estáticos , el O3 es un una Molecula Paramagnetico,generando Tensión superficial-como la Nata de la Leche u del agua en los ríos, razon porque los zancudos se desplazan en la superficie del aguyua estancada.
Quiero saber si es inflamable, si estando acumulado en una habitación, puede encenderse al prender la luz, como ocurre con otros gases. Gracias.
No lo sé Celeste.
Necesito saber las propiedades físicas y químicas del ozono 🥲para un trabajo
Hola. Googlelo. Más fácil y datos exactos.