En este artículo expondremos las Reglas de solubilidad, es decir, como darnos cuenta cuando un compuesto es soluble o no en agua. Entendemos que un compuesto es soluble en agua cuando por lo menos un gramo de este se solubiliza en 10 ml de agua.
Reglas de Solubilidad
Para facilitar el análisis, a continuación, presentamos un resumen de las reglas generales de solubilidad de los compuestos más comunes en agua, junto con sus principales excepciones:
| REGLAS DE LA SOLUBILIDAD | EXCEPCION |
| Los nitratos y acetatos son solubles | El acetato de plata es insoluble |
| Los compuestos de metales alcalinos son solubles y también los de amonio. | No hay. |
| Yoduros, cloruros y bromuros son solubles | Los de Plata, Pomo y Mercurio insolubles |
| Los sulfatos son solubles | Los de metales alcalinos y el de amonio son solubles |
| Sulfitos y Carbonatos son solubles | Los alcalinos y los de amonio son solubles |
| Los sulfuros son insolubles | Los alcalinos y los de amonio son solubles |
| Los hidróxidos y óxidos son insolubles | Los alcalinos y los de amonio son solubles |
Estas reglas de solubilidad, por otra parte, son importantes cuando estamos frente a una reacción química para saber si se formará o no una sustancia que precipite (insoluble) o no.
Veremos algunos ejemplos de reacciones moleculares y iónicas.
Hidróxido de sodio + Cloruro de Aluminio > Cloruro de sodio + Hidróxido de Aluminio
NaOH + AlCl3 > NaCl + Al(OH)3
Na+ + 3 OH– + Al+3 + 3 Cl– > Na+ + Cl– + Al(OH)3
Como vemos, el hidróxido de aluminio en la ecuación iónica sigue apareciendo como molecular por ser un precipitado. Según las reglas expuestas anteriormente es insoluble.
Nitrato de Plomo + Ioduro de Potasio > Nitrato de Potasio + Ioduro de Plomo
Pb(NO3)2 + 2 KI > 2 KNO3 + PbI2
2 NO3– + Pb++ + 2 I– + 2 K+ > 2 NO3– + 2 K+ + PbI2
El ioduro plumboso es el precipitado formado en este caso.
En otras ocasiones se pueden formar sustancias volátiles en lugar de precipitados. En estos casos dichas sustancias tampoco tienen la forma iónica. Por ejemplo:
Carbonato de calcio + ácido clorhídrico > Cloruro de Calcio + Dióxido de Carbono + Agua
CaCO3 + 2 HCl > CaCl2 + CO2 + H2O
Ca++ + CO3-2 + 2 H+ + 2 Cl– > Ca++ + 2 Cl– + CO2 + H2O
Se forma el producto volátil dióxido de Carbono.
Artículos relacionados de Interés:
Estequiometría
Soluciones Químicas
Cinética Química

Hola quisiera saber que solvente es el necesario para disolver el compuesto clorito de sodio y cuantos gramos de este compuesto debo de mazar, para disolverlo con un volumen específico de disolvente y que se pueda cristalizar. Agradecería su respuesta.
Hola Constanza el mejor solvente es el agua sin dudas por ser un solvente polar para un soluto ionico. Si hay otro te averiguo
hola queria saber si me puede ayudar , con que puedo diluir o emulsionar oxido de aluminio para lograr un liquido para pulir aluminio? muchas gracias espero su respuesta
Publicare tu pregunta Diego. Haber si alguien experto en el tema responde
Como se explica la solubilidad de compuestos químicos en ácidos.
Las solubilidades son por compatibilidad química.
En la tabla me parece que hay un error con las excepciones..
dice que X es soluble con excepcion de Y que son solubles ¿? Los hidroxidos por ejemplo son solubles con excepcion a los que tienen alcalinos y amonio? o son insolubles pero solubles cuando tienen alcalinos o amonio..
Esta clarito. Los hidróxidos de los metales alcalinos son solubles. Son solubles o insolubles según con que metales esten unidos.
Me sirvió mucho el aporte, se agradece.
«JJ» tiene razón, en la tabla aparece esto (el antepenúltimo ítem):
REGLAS DE LA SOLUBILIDAD
Sulfitos y Carbonatos son solubles
EXCEPCION
Los alcalinos y los de amonio son solubles
Pareciera que no hay excepción o que alguno de los dos debería decir insolubles (supongo que por tu respuesta sería «Sulfitos y Carbonatos son insolubles»)
Es posible lo revisaré gracias por tu aporte.
Hola quisiera saber porque el koh se disuelve en etanol
Como puedo citar este articulo?
De donde extrajiste la informacion?
Citalo con la url o dirigite a este sitio. La información es confiable soy Bioquímico y tengo material del cual subo
Hola una pregunta, si yo tengo IK en exceso.. precipita Hg?? porque segun las reglas precipitaría HgI2, pero no se forma un complejo soluble el HgI4 2- ???
No creo porque hay mayor diferencia de electronegatividad entre el I y el K no creo que el mercurio desaloje al potasio ya que no es tan electropositivo
gracias por todo tu si sabes te felicito haces un gran labor en ayudarnos dios te cuide thank
Gracias igual para vos bendiciones
Buen dia. Me podrias ayudar con este ejercicio:
1,42 g de una muestra de un compuesto puro, con fórmula M2SO4, se disuelve completamente en agua y se trata con un exceso de solución de cloruro de bario, resultando en la precipitación de todo el ión sulfato como sulfato de bario. El precipitado se recolectó, secó y pesó 2,33 g. Determine la masa atómica de M e identifique M.
Si. A partir de los 2.33 grs sacas la cantidad de SO4 teniendo en cuenta el peso del mol o peso molecular de BaSO4 (sulfato de bario) que es 233.33 entonces de esta masa 96 grs son del SO4 (sulfato) por lo tanto de 2.33 grs 0.96 grs serán de SO4 y este viene de M2SO4. Sabiendo que la masa de SO4 es de 0.96 gramos la restamos de la masa original de 1.42 grs dando la diferencia la masa de M2 exclusiva. Dando 0.46 grs. Como los 0,96 grs de SO4 equivalen a los 96 grs de peso molecular. Los 0.46 equivaldran a 46 grs del metal (M). Como es M2 dividimos por 2 dando 23. Por lo tanto el PM de M es 23 o sea es el sodio (Na). M2SO4 = Na2SO4
Hola me podrías decir algunos ejemplos de compuestos que solubilizan en medio ácido alcalino, en procesos de intercambio y en agua. Gracias
quiero saber las conclusiones de la utilidad de las reglas de solubilidad de las sustancias por favor
me parece q no es correcta la informacion de q los carbonatos son solubles, menos lo del grupo 2a,ademas, depende del cation que lo componga
Si es correcta es de buena fuente
Buenas ElQui! Necesito una solucion de nitrato de plata 3mol, cuantos gramos tengo que disolver en un litro? y en 100ml? Muchaaas gracias!
Hola como 3 mol? 3 molar?
hola, queria saber cual de estos compuestos es mas soluble en agua y porque:
cloruro de bario o cloruro de calcio. me serviria mucho. gracias
Hola te soy sincero hay muy poca diferencia. Ambos tienen cloro y la diferencia esta entre el calcio y el bario. El mas electropositivo de ambos le dará mayor carácter iónico al compuesto y el d emayor carácter iónico será mas soluble en el agua. El Bario es mas electropositivo ya que la electronegatividad aumenta para abajo en el mismo grupo. Esas caracteriasticas las puedes leer en el post de propiedades periodicas de los elementos.
si tengo 10 ml de hipoclorito de sodio al 4% p/v cuanto debo vaciar en un matraz de aforo de 10ml para obtener 0.5% p/v de cloro gaseoso (forma activa)quien me puede ayudar
Es un problema interesante. Primero debes hacer bien la reacción de generación de cloro gaseoso a partir de hipoclorito y asi entenderas el proceso.
2 ClO- —> Cl2
Necesitamos el doble de concentración de hiocorito con respecto al cloro. Entonces, si vos queres 0,5% de cloro necesitaras el 1% de hipoclorito. este 1% lo obtendras a partir de 4% del otro q es mas concentrado. Entonces usamos la fórmula. C1 x V1 = C2 x V2 donde habra q calcular q volumen del mas concentrado usare para hacer 10 ml del menos concentrado. 4% x V1 = 1% x 10 ml y listo. V1 = 1% x 10 ml / 4% V1 = 2.5 ml. Entonces medis 2,5 ml y lo completas con agua destilada hasta 10 ml y asi tenes 10 ml de cloro al 0,5% p/v
Es un problema interesante. Primero debes hacer bien la reacción de generación de cloro gaseoso a partir de hipoclorito y asi entenderas el proceso.
2 ClO- —> Cl2
Necesitamos el doble de concentración de hiocorito con respecto al cloro. Entonces, si vos queres 0,5% de cloro necesitaras el 1% de hipoclorito. este 1% lo obtendras a partir de 4% del otro q es mas concentrado. Entonces usamos la fórmula. C1 x V1 = C2 x V2 donde habra q calcular q volumen del mas concentrado usare para hacer 10 ml del menos concentrado. 4% x V1 = 1% x 10 ml y listo. V1 = 1% x 10 ml / 4% V1 = 2.5 ml. Entonces medis 2,5 ml y lo completas con agua destilada hasta 10 ml y asi tenes 10 ml de cloro al 0,5% p/v
Hola,una pregunta, por que el LiCl es soluble en agua y acetona mientras que el LiF es practicamente insoluble en agua?
Hola. Es una pregunta interesante. La diferencia esta en el fluor evidentemente. Pero no hay material que de esta exlicación. Por lo menos no lo encontre.
esta muy weno 🙂
Hola, tengo carbonato de calcio y ácido clorhídrico (al 33%). La ecuación que mostraste en el final, resulta una especie de carbonato de calcio líquido ? de ser así que cantidad de ácido clorhídrico (33%) se utilizaría para 100 gramos de Carbonato de calcio?
este sitio web es muy bueno!
Hola, bueno deberías plantear la reacción y ver después de balancearla. Para un mol de CO3Ca necesitarías dos de HCl. Así que si el peso molecular del CO3Ca es 100 grs necesitarás 73 gramos del ácido HCl. Pero como es líquido el HCl necesitarás la densidad aparte del % de pureza.
Hola Elquimico. gracias por la respuesta. bueno el HCL que tengo tiene un a densidad de 1,15 g/ml, y es al 33%.
Lo que me interesa mucho es hacer dos cosas:
1) Carbonato de calcio líquido
2) Caolín Líquido.
Crees que se pueda llegar con este HCl que tengo?
Saludos !
Vos queres hacer esas sales?. No veo para que queres al HCL entonces. No te servirá.
No quiero hacer sales.
Los tengo en polvo, tanto el caolín como el carbonato de calcio.
Y quisiera un suspensión. para poder aplicar en forma de spray.
Vi que ambos son muy insolubles en agua, y en la página vi que reaccionabas el carbonato con el HCl.
Por eso te pregunto.
Saludos!
Insolubles en agua?. Entonces proba con algún alcohol o solvente orgánico.
Quiero saber la solubilidad del sulfato de zinc al 36 % monohidratado
por favor ayudenme con este problema no lo encuentro en ninguna parte se disuelven 10g de hidroxido de aluminio en 100ml de agua hallarpeso a peso , peso a volumen , cuantas moles de soluto de disuelven , cuantos equivalentes de soluto se disolvieron , hallar molaridad, y normalida por favor aaaaaaaayuuuuuuuuuuuuddeeennnmmmmmeee gracias
Alejandro los problemas no los encontraras en ningun lado. Pero si estudias y entendes la teoría harás cualquier o la mayoría de los problemas.
Por ej:
10 grs en 100 ml de agua. Cada ml equivale a un gramo. O sea que en total sumando las masas de soluto y solvente (agua) tenés 110 grs de solución. Por lo tanto el % m/m será de:
10 grs de soluto / 110 grs de solución x 100 = 9.09 % masa en masa
% v/v ( volumen en volumen ) es algo parecido. podemos considerar que los 10 grs de soluto no tiene volumen entonces el volumen lo darán los 100 ml de agua.
Estudia mas por favor.
10 grs soluto / 100 ml de solución x 100 = 10 % v/v.
1_ porque el carbonato de calcio no es soluble en agua y presipita? (El carbonato de calcio)
2_porque cuando el carbonato de calcio reacciona con acido clorhidrico, el carbonato ed soluble en agua?
Porfa ayudame con las preguntas!!
Si puedo te lo averiguo.
Por que el carbonato de aluminio y el cianuro de aluminio no existen en soluciones acuosas??
No lo sabía
si la sacarosa es soluble en agua ¿por qué no conduce la corriente eléctrica?
Porque la sacarosa no es un soluto no disociable, es decir, no se separa en iones, por lo tanto al no haber iones no habrá forma de conducir la corriente eléctrica.
gracias
¿por qué los compuestos iónicos al estado fundido conducen la corriente eléctrica?
por estar más expuestos al ser otro estado físico.
Cómo varía la solubilidad de los metales alcalinos y alcalinotérreos al descender en el grupo?
Hola, es una buena pregunta, creería que mientras mas descendes en el grupo más reactivo se hace el elemento. Por lo tanto más soluble
Una consulta, si tengo una solucion de salmuera que contiene Na+, K+, Mg2+, Ca2+, Li+, (SO4)2-, CO3-, NO3-, Cl- y algunos otros en menor cantidad. Como puedo hacer para precipitar al magnesio, utilizando algun reactivo pero que sea de menor costo, tampoco puedo utilizar del Ca(OH)2 que resulta ser lo mas barato posible, ni un reactivo como el sulfato de bario, que es un reactivo muy costoso. Agradeceria mucho tu opinion
Complicado Moises vere que te averiguo
Hola MOISES se puede hacer precipitar al magnesio adicionando hidróxido de sodio a la solución, teniendo encenta que el anión que acompañe al magnesio en la solución (sal de magnesio o compuesto de magnesio soluble) tenga menor actividad que el ion carbonato de lo contrario el magnesio ya estaria precipitado en forma de carbonato de magnesio. si se adiciona NaOH precipitaría el magnesio en forma de Mg(OH)2
Una consulta: En el método de Vohlard para valorar Cl- con AgNO3 (exceso), y después el exceso de AgNO3 que queda sin reaccionar se valora con solución de SCN-. No entiendo porque dice que: «Ocurre que por ser el AgSCN más insoluble que el AgCl, el SCN- además de reaccionar con el exceso de AgNO3, ataca al AgCl disolviéndolo… AgCl+SCN- ———–> AgSCN+Cl-.» No entiendo porque se disuelve el AgCl.
Seguramente es porque deja en libertad iones cloruro haciendo disminuir el producto de solubilidad del cloruro de plata
cuales compuestos se solubilizan en agua o en hexano y porque ?
-cloruro de sodio
-fosfato de calcio
-azúcar de mesa
-naftaleno
-Etilenglicol, C2H6O2
-aceite
Hola. Cloruro de sodio, azúcar y fosfato de calcio si se solubilizan. El resto son insolubles
Muchas gracias
hola buenos dias me gustaria saber que solvente puedo utilizar para el sulfato doble de aluminio y amonio
Hola, no lo sé. Si encuentro algo te digo.
Hola, me gustaría saber que otros solventes sencillos a excepción del agua se puedan utilizar en una solución ionica no polar.
Hola el agua es polar. Otros polares son algunos alcoholes como el metanol o etanol. Vos queres no polares?.
hola patricio espero que te encuentres bien… quiero que me ayudes que puede exponer en clases sobre el tema reglas generales de solubilidad
Hola Héctor saca material tranquilo puse lo básico
Podrías apoyarme enlistando todos los elementos de la tabla periódica que son solubles en agua
y cuales sirven como conductor de electricidad.
Nota: como elementos solos, sin compuestos. Gracias
David no hago ejercicios tan extensos. Es una cuestión de tiempo, imaginate que les responda a todos algo tan largo
Hola quiero saber si el nitrato de lantano es soluble en agua y si lo es cuantos gramos necesito para disolverlos en 100ml de agua?
No sabria decirte si es soluble o no, no tengo esa información.
El CaCo3 es soluble en agua? ¿Y el KNO3?
¿Cómo lo puedo comprovar?
Gracias
Hacete una solución en agua con esas dos sales
Hola Patricio, yo tengo una pregunta. Qué se espera que se disuelva mejor en agua el NaCl o el Na2SO4 y por qué?
Gracias de antemano
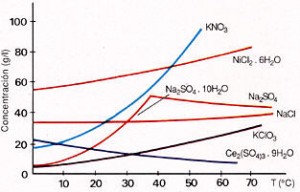
Hola, tengo entendido que el NaCl pero las razones exactas no las sé. Fijate en el gráfico que publique. El ClNa se disuelve más, pero a partir de cierta temperatura el sulfato es más soluble.
Hola! Tengo problemas para solubilizar un Fosfato de calcio Ca3(PO4)2 en agua, necesito que conserve su estructura molecular ya que debo agregarlo a un medio de cultivo. Espero que me puedas ayudar.Gracias
aha interesante. Nose exactamente pero deberías agregar otra sustancia. Si averiguo te lo mando.
Hola, me gustaría saber las constantes de solubilización en agua del oxigeno, nitrógeno y dióxido de carbono. Busqué en todos lados pero no he conseguido nada claro, agradecería mucho tu ayuda. Saludos
Dejemos esto publicado a ver si alguien las conssigue
¿por que varia tanto la solubilidad de los metales?
Depende la la electropositividad. Los del grupo 1 y 2 son mas electropositivos, se ionizan mas y se solubilizan mas en el agua que es un solvente polar.
Hola, me gustaria saber porque el sulfato se magnesio es soluble en agua y al descender en el grupo del magnesio esta solubilidad es escasa. Por ejemplo, el sulfato de bario es muy poco soluble. ¿A que se debe esta propiedad?
Saludos!
Hola francamente no lo se con exactitud pero creo que tiene que ver con el radio atómico.
perdón quise decir por que varia tanto la solubilidad de los no metales ?
Buenos días, Si se tienen dos soluciones saturadas de NaCl y de potasio KCl en agua a 40 °C de temperatura y se enfrían ¿Qué sal precipita antes? ¿Por qué?
hola, buenos dias me podrias ayudar ya que no se nada de quimica cual de estas sustancias es la menos soluble en agua a) sulfatos b) nitratos c) bromuros d) acetatos e) carbonatos
Segui las reglas que explique en el post
Buenas tardes Patricio, tengo una duda bastante básica, pero encuentro información que se contradice y la verdad es que me estoy volviendo un poco loca, le explico:
Sobre el sulfato cálcico y las reglas de solubilidad, he encontrado en diversa bibliografía que se trata de una sal insoluble («son solubles todos los sulfatos excepto los de calcio, estroncio, bario, plomo y plata»), encontrando datos en los que aportan que su solubilidad es de 0,24 gr/l (muy escasa). Sin embargo, en otros manuales he encontrado que el sulfato cálcico es soluble (por ejemplo, se utiliza en ocasiones como nutriente agrícola para suelos) con un índice bastante más alto de solubilidad.
En definitiva, imagino que tendrá relación con la forma en la que el sulfato cálcico se presenta (hidrato, semihidrato, anhidro…) pero no consigo saber exactamente en qué caso se trata de una sal soluble o insoluble. ¿Podría aclararme esta duda?
No, pero creo que se atribuye a lsa condiciones distintas como decís. Si es hidratado por ejemplo. Aparte en el suelo es diferente que en el agua
describe dos Suspensiones describiendo las Características generales de su conformación en
relación a las partículas que la componen y su solvente.
Una pregunta el carbonato de calcio y el bicarbonato de sodio son solubles en eter de ser asi por que?? gracias
No lo sé dejemos la pregunta publicada por si alguien aporta algo.
Buenas tardes,
¿en qué otros compuestos -diferente al agua- o químicos es soluble el bicarbonato de calcio?
buenos días. quisiera preguntarte porque en la reacción de nitrato de plata al agregarle hidróxido de sodio me da un color marrón opaco ? eso se debe a que ?
No lo sé.
Hola Patricio, me podrías decir el grado o si es soluble el Yoduro de sodio en alcohol etílico 96°. Te agradezco de antemano.
Hola Abel no lo sé.
Oye una pregunta: ¿Por qué el yoduro de potasio no es soluble en el sodio???
El sodio ni siquiera es solvente
¿Cual es tu apellido para poder citarte?
Mi nombre: Patricio Arroyo
¿Cuál es la razón por la cual la mayoría de los compuestos de los metales alcalinos son solubles en agua?
El agua es un solvente polar. Eso hace que sea más compatible con metales que forman iones como los del grupo 1 y 2
Buenos días, quiero saber si los siguientes compuestos son solubles o insolubles en agua, empleando la regla de solubilidad
NiCl2
Ag2S
Cs3PO4
SrCO3
(NH4)2SO4
Quisiera saber dependiendo de qué los elementos son solubles con respecto a la posición en la tabla periódica?
La solubilidad no tiene que ver con la posición en la tabla sino con la afinidad que haya entre soluto y solvente.
Hola me dieron este ejercicio y no lo logro entender me podrias ayudar por favor
Un elemento químico tiene 2 isótopos: uno de número másico 54 que está presente en una abundancia de un 2,3 %. Si el número másico del otro isótopo es 56:
a) Determine el peso atómico del elemento.
b) Si una muestra de 10,43 gramos tiene un 5,2 % del elemento, determine cuántos átomos del isótopo de A=56 habrán en la muestra.
c) Si el elemento posee 26 protones, clasifíquelo de acuerdo a su configuración electrónica.
Hay una fórmula que no recuerdo bien pero debes multiplicar a ambos pesos atómicos por sus porcentajes de aparición y luego dividirlos por 100.
Sería:
54 x 2,3 + 56 x 97,7 / 100 =
Hola, quisiera saber porque la insolubilidad del carbonato de calcio y como se clasifica la reaccion
insolubilidad en que
Hola muy buenos días. Tengo una duda y me gustaria ponerla en practica por afición.
Tengo una caja de pastillas que su principio activo es el Bupropion, marca (Elontril), pero estas pastillas también contienen Poli (alcohol vinílico), dibehenato de glicerol. Cual es el método para separar estas 3 sustancias por separado. Se hace jugando con la solubilidad.
Composición:
150mg Bupropion
Los demás componentes: Poli (alcohol vinílico), dibehenato de glicerol
No tengo idea Diego es algo demasiado específico. Debe responderla alguien que trabaje en una industria farmacéutica
Hola.
¿Qué tipo de disolución se prepara cuando el bromato de sodio cuya solubilidad es de 36,4 g /100 g agua a 20ºC se calienta a 100ºc y se enfría hasta 20ºc?
Gracias
A que te referís?. Si es saturada o diluída?.
BUENAS TARDES ME PODRIAS EXPLICAR QUE SIGNIFICA QUE EN EL SACO DE UN FERTILIZANTE DIGA QUE TIENE CALCIO SOLUBLE EN HCL 18%, QUIERO SABER SI ESTE FERTILIZANTE SI ES SOLUBLE EN EL SUELO AL MOMENTO DE LA APLICACIÓN Y SI LA PLANTA SI ES CAPAZ DE ABSORBERLO.
MUCHAS GRACIAS
Hola, no soy experto en fisiología de plantas.
tienes canal de youtube?
Hola. Por supuesto buscame como ElSanto y verás artículos de Química, Física y Matemática
Hola! Necesito saturar acetona y Dimetilsulfoxido con CaCo3. Qué cantidades necesito o cuál es la solubilidad del CACO3 en estos solventes? Gracias de antemano.
Hola. Ni idea pero dejo tu pregunta a ver si algún experto la sabe.
Hola me gustaria saber la solubilidad del acido fenilglioxilico en agua
Hola, me gustaría saber cual es la ley de la solubiliadad
No hay una ley específica. La solubilidad depende de varios factores como temperatura, composición química, etc.
buenas ,necesito saber dos sustancias practicamente insoluble en agua que se usen diariamente en el hogar.si me puedes ayudar te lo agradeceria porque es para una tarea evaluativa
aceite y tierra
Hola me podrías decir algunos ejemplos de compuestos que solubilizan en medio ácido alcalino, en procesos de intercambio y en agua, cuál sería la ecuación del proceso. Gracias
No te entiendo y creo no saberla pero la publicare a ver si alguien te entiende.
hola me podía colaborar con estos ejercicios
balancear por el metodo algebraico y nombrar todas las sustancias de las sgt reacciones
1. Mn(NO3)2+K2SiO3+Mn2S3 produce K2SO4+SiO3+K2MnO4+NO+K2MnO4
2.KMnO4+BiBr2+H2SO4 produce Br2+MnSO4+K2SO4+Bi2(SO4)3+ H2O
Hola Santiago no colaboramos por razones de tiempo. Por eso cobramos este tipo de trabajos. Abrazo.
Hola, una pregunta como sé si el compuesto químico NH4+ es un compuesto soluble, insoluble o metal alcalino?
hola una pregunta Explique por qué una proteína es soluble en un hidróxido alcalino y es insoluble en un ácido inorgánico.
No todas las proteínas son iguales. Algunas tienen tendencia a solubilizarse en medio ácido y otras en medio básico, esto depende de sus grupos químicos expuestos en la molécula.
¿Cómo explicar la solubilidad o insolubilidad basada en la estructura molecular y polaridad?
0,5 gramos de soluto con 2 ml de solvente:
-azúcar con agua destilada
-sal con cetona
-Potasio con etanol
– 2 gramos de Tiosulfato de sodio pentahidratado con 5 gotas de agua destilada.
Agradezco su respuesta. Sé que es idóneo y podrá ayudarme. Excelente contenido. Gracias.
La solubilidad depende de la compatibilidad química entre soluto y solvente. Por ejemplo si ambos son polares serán más solubles.
Que es la solubilidad de un compuesto?
La cantidad de soluto que admite un solvente. Y varía según la temperatura.
Hola alguien que me ayude con este ejercicio
1) La KPS de hidróxido de calcio es 1.3 x 10-6. ¿Esperaría que precipite hidróxido de calcio si mezcla 2 Litros de cloruro de calcio 0.050 M con 0.5 L de hidróxido de sodio 0.5 M?
Desde ya gracias
Saludos
Hola, como sabría si algunos compuestos son mas solubles en ácido o en agua? Gracias
Hola, me gustaría saber como afecta la solubilidad de un soluto cuando se añade otro.
En este caso se trata de acido azelaico en agua ¿Como afecta añadir otro soluto (acido pelargónico) a la mezcla?
¿Disminuiría la solubilidad de cada uno de los solutos siendo la solubilidad total un valor intermedio?
Gracias.
Un saludo.
Multiplica 3.75 moles por el peso molecular.
Buen dia; disculpa quizas no es el tema para esta pregunta pero te pido me ayudes con esta duda que tengo desde hace muchos años, necesito saber si existe una sustancia llamada ENANTATO DE CALCIO, y como se obtiene.
Gracias
Daniel PH
Hola Dani. Perdona nunca la escuche.
¿Por que los compuestos ionicos no son solubles en solventes no polares?
Porque no son compatibles químicamente. Por lo tanto no hay fueras de asociación entre sus moléculas. Sino más bien re repulsión.
Buenos días,
He visto que el óxido de magnesio es soluble en amoniaco. Si disuelvo el óxido en una disolución de amoniaco, ¿Qué reacciones tienen lugar?
Gracias
Hola. No lo sé. Esa reacción no la he visto.
Alguien puede balancear estas ecuaciones. No se de quimica mucho .
C2H6O2 + NaCl. Si le agrego glicerol quedaria asi. C2H6O2 + NaCl + C3H8O3. Se desprende hidrógeno?. Es una solucion para electropulido de acero inox Sinembargo explotan las burbujas de hidrogeno formadas en el proceso. Lo evitaria la glicerina (glicerol)?
Te faltan los productos. Igual te la publico.
Hola! Te felicito por tu página y por la buena disposición que tienes para responder todas las consultas que te llega.
Quisiera pedir tu ayuda. Necesito saber si cloruro de sodio y sulfato de calcio son solubles en etanol. Muchas gracias!
No lo experimente Paula querida. Pero creo que si porque son solutos polares en un solvente polar. Te invito a mi canal
https://www.youtube.com/channel/UCWzKIkF6_U4poswb9qgfVgQ
Hola quisiera saber que solvente es el necesario para disolver el Carbonato de propileno, dimetiil carbonato (DMC), etil carbonato y cuantos ml de este compuesto es necesario para disolverlo con un volumen específico de disolvente . Agradecería su respuesta.
Hola. No conozco esos compuestos pero te dejo publicada la pregunta por si alguien aparece.
tengo una consulta que compuestos se solubilizan en alcohol
deben ser iónicos o polares y de peso molecular no tan grande.
Hola, me pide la solubilidad (solvente) en gráfica del manganeso, cómo puedo hacer ? no tengo ni idea, muchas gracias
No buscaste en google como graficas de solubilidad?.
Hoola, quiero saber que pasa si un elemento es soluble y el otro no? que seria al final solido o acuoso?
Hola. Es soluble o insoluble.
Hola, hay una regla general de solubilidad? Y si la hay, cuál es?
Hola. No