Los núcleos de los átomos de algunos elementos tienen la propiedad de emitir radiaciones. Podemos diferenciar básicamente dos tipos de radiaciones de los núcleos de elementos radioactivos. Partículas y rayos. Dentro de las partículas tenemos a las α (alfa) y las β (beta). Y de los rayos citaremos a los gama.
Las partículas α son iones helio o sea átomos de helio que han perdido sus dos electrones. Por este motivo queda cargado con dos cargas positivas.
He – 2e- —-> He ++
Por consiguiente las partículas alfa están formadas por núcleos de Helio.
Las partículas beta están formadas por electrones. O sea, tienen una carga negativa y carecen de masa.
Rayos gama: Son radiaciones electromagnéticas de frecuencia más elevada que los rayos X, es decir, tienen menor longitud de onda.
Citaremos las propiedades más importantes de los elementos radioactivos:
1) La radioactividad es considerada una propiedad atómica, y se da en los átomos más inestables.
2) Estos átomos inestables se desintegran emitiendo los distintos tipos de radiaciones mencionadas anteriormente.
3) Los elementos radioactivos se están transformando continuamente en elementos más estables.
Radioactividad natural.
El proceso de radioactividad no es necesariamente artificial, ya que se da también de forma natura. Es la transmutación espontánea de un elemento a otro.
Ejemplo:
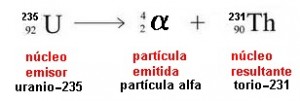
El Radio emite una partícula alfa transformándose en una sustancia de peso atómico 4 unidades menor y de número atómico 2 unidades menor llamada Radón (Rn).
Otro ejemplo es la desintegración del Uranio radioactivo
Observamos que la perdida de una partícula alfa hace disminuir el número atómico en 4 unidades y el másico en 2.
El Torio producido también es radioactivo e inestable, por lo tanto se desintegra en:
Aquí vemos que la pérdida de un electrón beta del átomo aumenta el número atómico (Z) en una unidad pero no modifica nada al número másico (A). al parecer un neutrón se transforma en un protón y un electrón. Este electrón es expulsado como partícula beta.
Podemos concluir que en una transformación radioactiva cuando se emite una partícula alfa, el producto está desplazado dos grupos hacia la izquierda de la tabla periódica y si la emisión se trata de una partícula beta el desplazamiento es de un grupo hacia la derecha.
Cuando un elemento radioactivo emite una partícula alfa y 2 partículas beta, su Z no varía pero si cambia su (A). Entonces se obtiene un isómero del elemento.
Series radioactivas:
Son aquellas en las cuales los elementos sufren sucesivas desintegraciones y van transmutándose hasta llegar a un mismo isotopo. Todos estos pasos constituyen la serie radioactiva. Como ejemplos podemos citar a 3 muy conocidas.
Serie del Uranio: El Uranio se transforma en Plomo.
Serie del Torio: El Torio se transforma en Plomo.
Serie del Actinio: El Actinio se transforma en Plomo.
Los elementos Plomo así obtenidos son isotopos.
Todos ellos tendrán como número atómico 82. Pero El Pb del Uranio será de 210 de masa, el Pb del Torio 208 y el Pb del Actinio 207. Son isótopos entre si.
Vida Media:
Un concepto muy importante que se aplica con frecuencia es el del tiempo de vida media de una sustancia. Se llama así al tiempo necesario para que se desintegre la mitad de un material radioactivo.
Este puede varias desde unos escasos segundos hasta millones de años. Por eso las unidades pueden variar en: a (años), m (meses), d (días), h (horas) y s (segundos).
Transmutación artificial:
Mientras que la transmutación natural se conoce desde 1895, la artificial fue hecha por primera vez por Lord Rutherford, quien bombardeando nitrógeno con partículas alfa obtuvo oxígeno:
![]()
A continuación veremos otro ejemplo donde se indican transmutaciones bombardeando átomos con neutrones.
Radioactividad Artificial:
En el año 1934 los esposos Curie observaron que bombardeando magnesio con partículas alfa se obtenía un isótopo inestable del Silicio.
![]()
Este isótopo del Silicio es radioactivo. Y se desintegra emitiendo positrones que son los electrones positivos.

Esto es la radioactividad artificial o también llamada Inducida. Cuando se bombardean átomos de algunos elementos para producir otros, pero radioactivos.
Fisión nuclear.
En 1938 se descubrió un nuevo tipo de reacción nuclear. Consiste en el bombardeo de ciertos núcleos que se rompen en dos partes aproximadamente iguales liberando una gran cantidad de energía, mucho mayor que la que se produce en la radioactividad ordinaria.
En las partes resultantes de la fisión hay una baja de la masa que se transforma en energía según la ecuación de Einstein. E = m x c2.
Esto significa que en la fisión pequeñas masas liberan enormes cantidades de energía. Muchísimo más de lo que sucede en reacciones ordinarias.
Han y Meitner bombardearon átomos de Uranio con neutrones y obtuvieron:
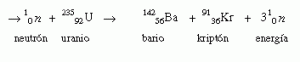
Los neutrones que se liberan bombardean nuevos átomos y los desintegran.
Estos átomos al desintegrarse dejan libres nuevos neutrones que a su vez repiten el fenómeno produciéndose una reacción en Cadena.
Reacción en cadena.
La reacción en cadena libera una gran energía en muy poco tiempo. Las reacciones en cadena pueden ser de dos tipos.
Reacciones nucleares no controladas.
La reacción es violenta como es el caso de la bomba atómica.
Reacciones nucleares no controladas.
La velocidad de reacción se regula disminuyendo la velocidad de los neutrones que producen la reacción de fisión.
Ello se logra con un reactor en el que se intercala grafito, cadmio, agua pesada, etc.
La gran cantidad de calor producida, se usa en muchas aplicaciones. Como mover motores, girar turbinas para producir energía eléctrica a través de un generador.
Aplicaciones de los Isótopos radioactivos.
Tienen muchos usos, como en la Agricultura, Medicina, Industria, etc.
En medicina se emplean debido a que presentan afinidad específica por diversos órganos, glándulas o tejidos en los que se localizan. Por ejemplo, el Yodo radioactivo tiene afinidad por la Tiroides, el hierro radioactivo por la hemoglobina, el fósforo por los dientes y huesos, etc. este último se usa también para combatir la leucemia y el carbono radioactivo para el cáncer. Estas son solo algunas de las innumerables aplicaciones que cada vez son más en la utilización de isótopos radioactivos. Aparte el uso de marcadores radioactivos ha permitido estudiar y conocer mejor al metabolismo celular y entender procesos como la fotosíntesis y otros que parecían muy complejos.
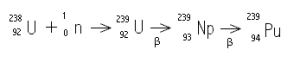

no me gusta necesitos donde fue radioactividad o algo asi
Como donde fue? Explicate mejor
quiero saber un compuestos radiactivos que hacen reacciones quimicas xq busco y busco y no sale nada alguna ayuda de compuestos o elemntos sin graficos porfavor urgente
Podrias ser mas esecifico?
Quiesiera saber las aplicaciones en la vida cotidiana, por ejemplo en la medicina, agricultura, etc…
yo pieso o miso ue tu io
que se hacen de que saben hijos de puta
No saben ni mierda encima ocultan muchas cosas acerca de la radioctivad
Primero sos un mal educado aca no se insulta a nadie. Y no se oculta info ahora si vos podes aportar algo q ovbiamente no creo q puedas hacelo sino no hables estupideces
encontré buena y formación pero sean mas especificosssss si porfa
Muy buena la explicación, bastante simple para personas ajenas al entusiasmo del conocimiento. Aunque falto un poco mas de contenido. GRACIAS.
necesito saber que son y para que sirven las particulas alfa y beta
las particulas alfa son nucleos de helio (2 p , 2 n )
Hola, quisiera saber que es la desintegración nuclear y como funciona un reactor nuclear. ¿Podrias ayudarme?
Que tema Maca, sinceramente no soy experto en el tema.
Desintegración nuclear te lo dice la palabra. Se bombardea el nucleo con partículas a alta velocidad, como neutrones hasta que se desintegra el núcleo en fragmentos mas pequeños.
me podria ayudar en :
las transmutaciones artificiales han permitido obtener elementos sinteticos como el curio-242, que se produce bombardeando plutonio-239 con particulas alfa. ¿Que otra particula se emite?
pues hay podia escribir que ss elemnetos atomicos ie prodcen bombardeos con alfa
Quiero saber dos ejemplos de la radiactividad y sus aplicaciones en la industria’?
xfa
Hola, a lo último del post dejo algunas aplicaciones industriales y medicinales.
necesito un listado de las 10 aplicaciones de la radioactividad
buenas tardes, mi profesor de química me dejo un taller acerca de esta lectura será que usted tiene las repuestas? muchas gracias
No creo Daniel es solo un post informativo
Hola soy física ,e imparto química , Biología y matemáticas y me gusta toda la información que enriquece mis conocimientos, me gusto el detalle que para el tipo de cáncer es diferente el tratamiento,gracias
Un beso Mara. Un gusto que gente de tu nivel comente en mi sitio.
hola chicas responden si quieren hablar
Hola, necesito saber como es que los rayos x, luego de ser absorbidos por los huesos forman imagenes y por que se utilizan los medios de contraste como iodo y bario en las radiografias?
Buena pregunta la publicare a ver si algún experto la contesta.
Si la radiactividad es una reacción que se da en el núcleo y se emiten partículas de éste, ¿por qué una de sus emisiones (las partículas beta) están formadas por electrones que entiendo no forman parte del núcleo si no de la «nube»?? o en todo caso ¿qué emite el núcleo que hace que se desprendan electrones de su «nube»?
No es que sean electrones sino que equivalen en carga
hablando en lenguaje molar y molecular cual es la diferencia
A que diferencia te refieres?.